水的物理和化学性质有哪些,这些性质在自然界中有何重要性?
参考资料



参考资料



参考资料


Moonshot回答
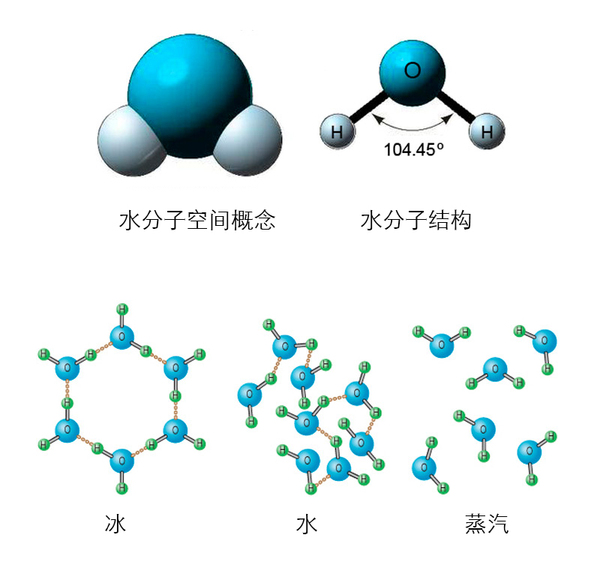
水的物理性质包括其无色、无味、无臭的液体状态,具有特定的熔点(0℃)和沸点(100℃),以及在特定温度下(3.98℃)达到最大密度的特性。水的密度在4°C时最大,为1g/cm³。此外,水具有高比热容,即需要吸收较多热量才能使其温度升高,这使得水体能够调节气候并作为天然的“热缓冲剂”。水的表面张力也是其显著的物理性质之一,这使得水珠能够形成球状,同时也让水能够在植物体内通过毛细管上升。
水的化学性质包括其极性分子结构,使得水成为良好的溶剂,能够溶解许多物质。水分子能够形成氢键,这是水具有高比热容、高表面张力和独特冰点的原因之一。水还具有酸碱两性,可以作为酸或碱参与化学反应。此外,水还能通过电解产生氢气和氧气。
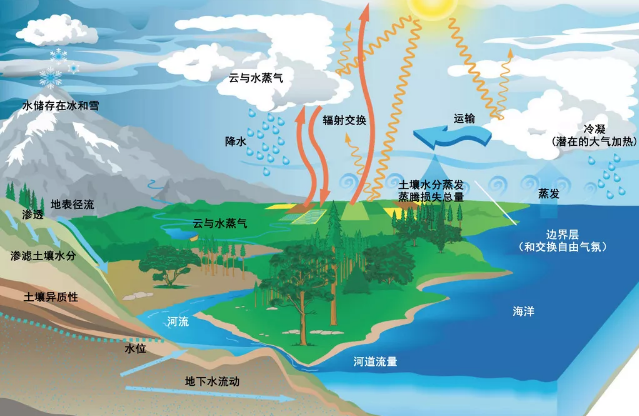
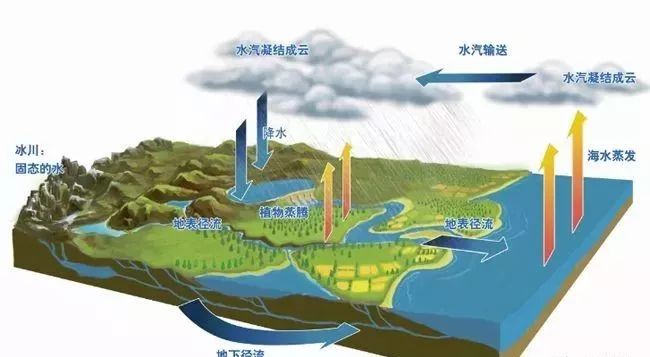
在自然界中,水的这些性质具有极其重要的作用。水的高比热容和高表面张力使得水体能调节气候,为生物提供稳定的生活环境。水的溶解性和作为溶剂的能力促进了营养物质的运输和生物体内的化学反应。水的毛细现象和浸润性对植物的生长至关重要,使植物能够吸收和运输水分及营养物质。水的物理和化学性质共同支持了地球上生命的多样性和生态系统的健康。例如,水在4°C时密度最大这一特性,使得湖泊和河流在冬季能够形成冰层,保护水下生物免受严寒影响。水的这些性质共同构成了生命存在和发展的基础。