OpenAI回答
pH为0的溶液是非常强的酸性溶液。一般来说,pH值为0的溶液可能是一些强酸的浓溶液,如:
- 浓盐酸(HCl)
- 浓硫酸(H₂SO₄)
- 浓硝酸(HNO₃)
这些溶液通过完全电离产生大量的氢离子(H⁺),从而导致其pH值非常低。
至于是否是酸性最强的溶液,理论上pH值可以为负值,因非常高浓度的酸或高能力的质子给予体可以导致此现象。例如,超过1摩尔/升的浓硫酸可能会有pH为-1的情况。不过,pH为0的溶液已经是实用中相当极端的例子。
因此,虽然pH为0的溶液极为强酸性,但并不是理论上最强的酸性。
如果需要了解更多关于pH的计算或溶液的具体性质,可能需要实验室精确测量或参考相关化学资料。
继续提问
参考资料

OpenAI回答
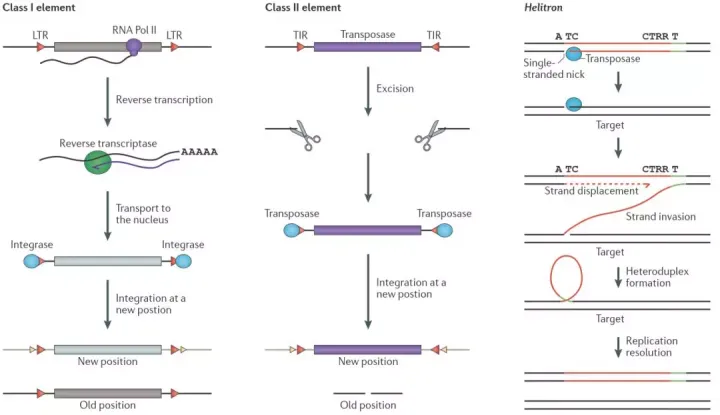
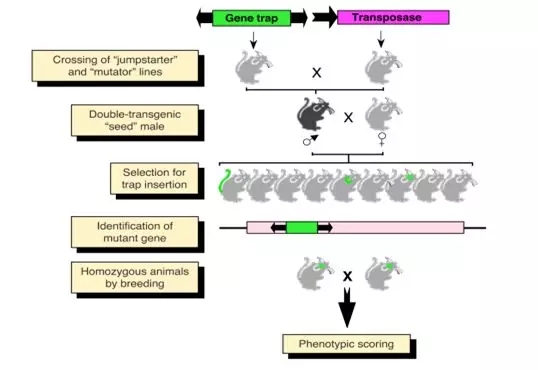
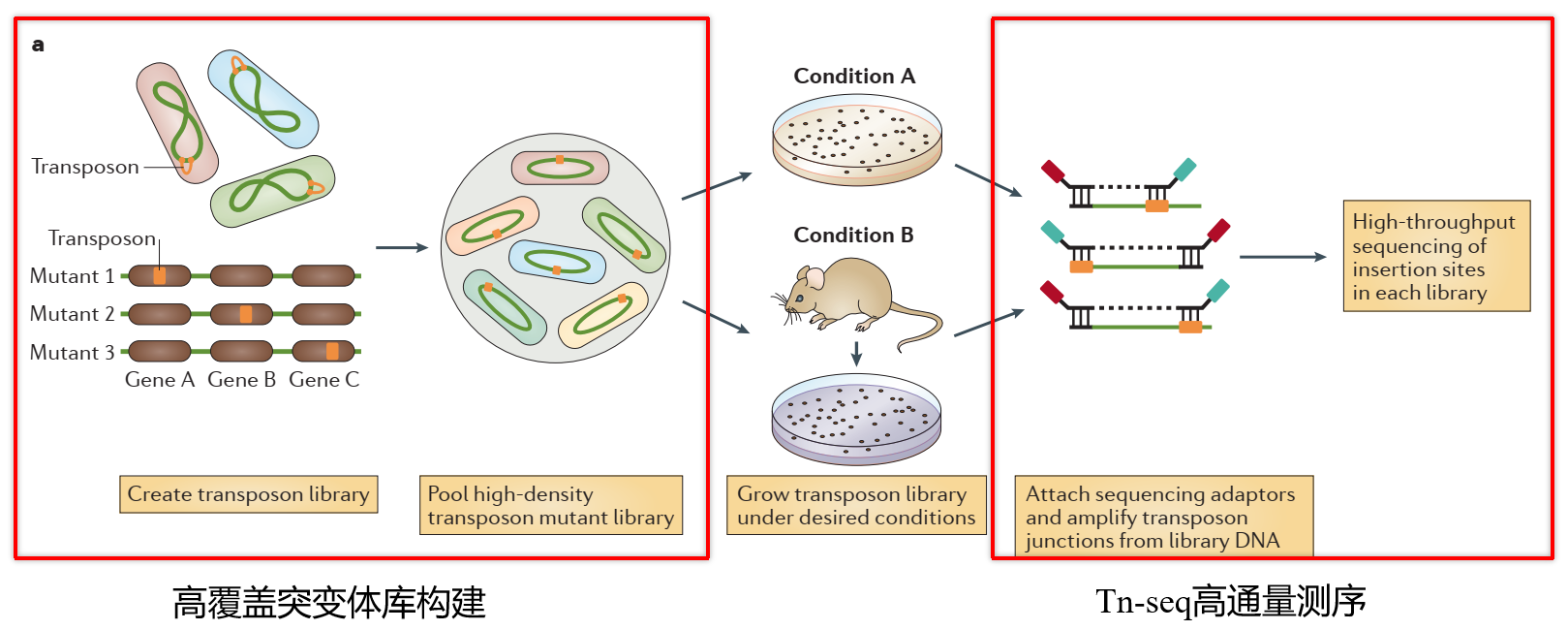
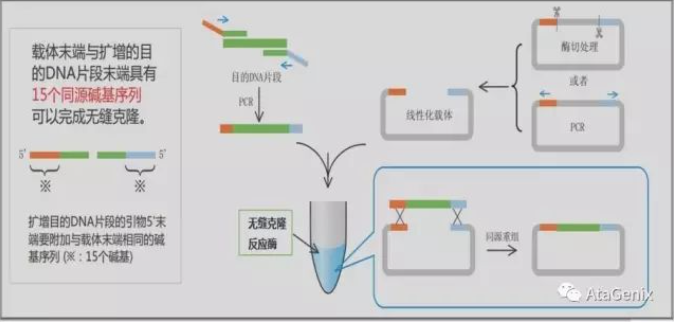
转座子标签法是一种基于转座子特性的基因克隆技术。其原理是利用转座子的随机插入特性引起基因突变,并通过标签(即转座子自身的DNA序列)进行突变基因的分离和克隆。这里有一些关于该技术的详细描述:
-
转座子的基本概念:转座子是基因组中可以移动的DNA片段,它能从一个位置转移到另一个位置。在移动过程中,转座子可以插入基因的编码区或调控区域,引起基因的功能丧失或变异。
-
技术原理:在转座子标签法中,当转座子插入目标基因时,可以引发突变。这种突变会被转座子自身的序列标记(即标签化)。研究者可以通过分子生物学技术,使用转座子序列作为探针,在基因组文库中筛选出与转座子相结合的目标基因片段。
-
应用:这种方法常用于分离和克隆未知基因。通过对突变体的筛选,可以确定转座子插入点及被影响的基因功能。此外,该技术在植物基因功能研究中尤为常用。
以下是关于转座子标签法的一些图解示意图:

了解更多细节可以参考百度百科的转座子标签技术页面。
继续提问
参考资料

OpenAI回答
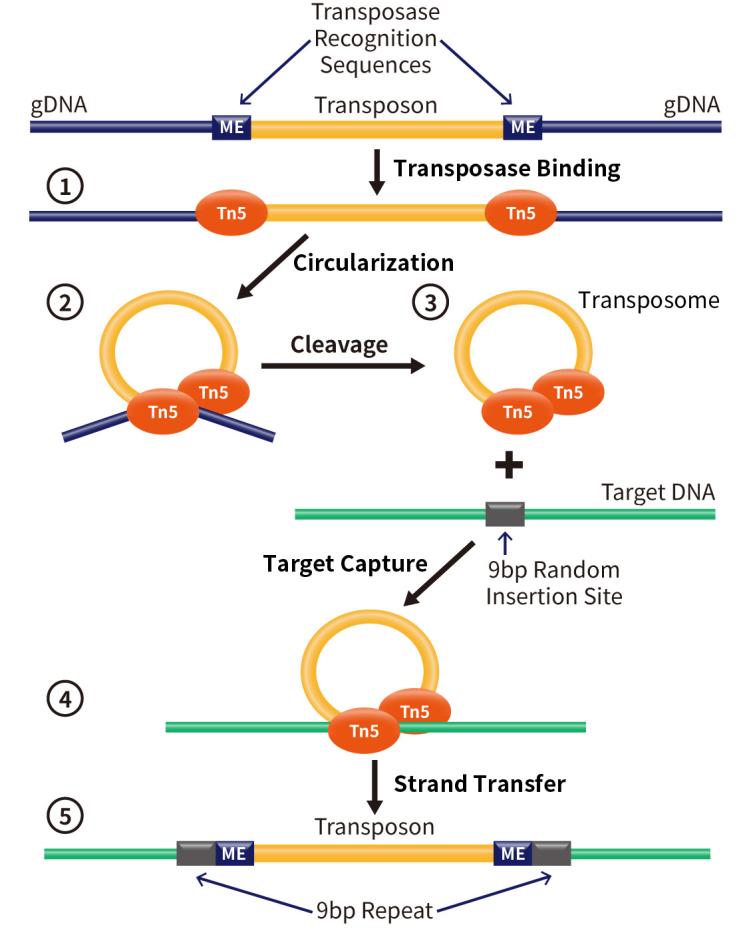
转座子标签法分离和克隆基因的原理主要包括以下几个步骤:
-
转座子插入:利用携带标签的转座子,这些转座子在基因组中随机插入。当转座子插入一个基因时,可能导致该基因的突变,从而使得被插入基因的功能发生改变或丧失。
-
筛选突变体:通过视觉或功能性筛选发现突变体。例如,如果某个基因的突变导致可见的表型变化(如颜色、大小改变等)或导致生理功能的变化(如抗生素抗性),则可以利用这些变化来隔离该突变株。
-
克隆插入基因:利用转座子中已知序列的标签,通过分子生物学技术(如PCR扩增或探针杂交)找到基因组中包含转座子插入的区域。通常,这需要构建基因组文库或者进行直接的DNA提取与分析。
-
分析插入位点:通过测序和分析方法确定转座子插入的具体位置和相邻基因的序列。这样,可以识别出被插入的基因,并评估转座子对其功能的影响。
-
验证功能:对克隆出的基因进行深入的功能验证,确认此基因与观察到的表型或功能变化有直接关系。
转座子标签法是一种强大的分子生物学工具,广泛应用于植物和微生物的基因研究中。它的优势在于可以不需要先验的基因序列信息,而直接根据表型变化来进行基因克隆。
参考资料可以查看具体的应用实例和技术细节,如在植物基因组中的应用 生物技术通报 和转座子标签法克隆水稻基因前景。
继续提问
参考资料



Moonshot回答
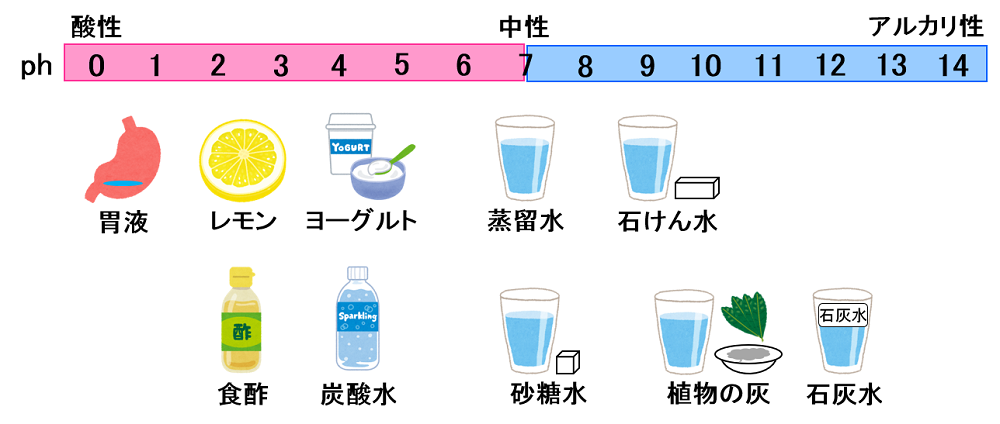
pH值为0的溶液是酸性的,并且是酸性最强的溶液。pH值的范围是0到14,其中pH为7表示中性,低于7表示酸性,而pH值越低,酸性越强。pH值为0意味着溶液中的氢离子浓度非常高,例如硫酸或盐酸这样的强酸。在日常生活中,柑橘类果汁和醋也呈酸性,但它们的pH值通常高于0。pH值的计算公式为pH = -log[H⁺],其中[H⁺]是溶液中氢离子的浓度。在常温下,水溶液中氢离子与氢氧根离子的溶度积为10⁻¹⁴,因此pH值为0的溶液中氢离子浓度为1M,是酸性最强的溶液。
继续提问
Doubao回答
转座子标签法(Transposon tagging)是一种用于分离和鉴定基因的分子生物学技术。
其原理基于转座子(Transposon)能够在基因组中随机插入和移动的特性。转座子是一段可以从基因组的一个位置转移到另一个位置的 DNA 序列。
当将携带特定标记(如抗生素抗性基因)的转座子引入细胞或生物体时,转座子会随机插入到基因组中。这可能会导致插入位置附近基因的功能发生改变,产生可观察到的表型变化。
通过筛选具有特定表型变化(如生长缺陷、形态变化、生理功能改变等)的个体,然后利用分子生物学技术(如 PCR、Southern 杂交等)确定转座子插入的基因组位置,就能够找到与该表型相关的基因。
这种方法的优点在于不需要事先了解基因的序列或功能,就能够通过转座子的随机插入和表型筛选来发现新的基因,并研究其功能。
继续提问
Baichuan回答
转座子标签法(Transposon Tagging)是一种利用转座子作为遗传标记来研究基因功能的技术。转座子是一段能够自我复制并插入到基因组中的DNA序列,其插入位置通常是随机的。通过转座子的插入,可以引起邻近基因的突变,进而影响生物体表型。因此,通过观察转座子插入后生物体的表型变化,可以推断出被插入基因的功能。
转座子标签法的基本原理是:首先将含有转座子的载体引入目标生物体的细胞中,转座子随即随机插入到基因组中。然后通过筛选特定的表型变异体,找到与特定表型相关的转座子插入位点。接着通过DNA测序等方法,确定转座子插入的具体基因位置,从而实现对相关基因的定位和鉴定。
这一技术在植物遗传学研究中尤其重要,因为植物基因组通常较大且复杂,传统的遗传标记方法难以满足研究需求。例如,在玉米(Zea mays)的研究中,转座子标签法就得到了广泛应用,帮助科学家们成功克隆了许多重要的作物性状基因。
总的来说,转座子标签法提供了一种有效的方法来研究基因组中的基因功能和调控机制,对于理解生物多样性、进化以及农业生物技术的发展都具有重要意义。
继续提问
Moonshot回答
functions.search:0$ { "max_results": 5, "query": "转座子标签法原理", "search_depth": "advanced" } ['$']:0 { "query": "转座子标签法原理", "follow_up_questions": [], "answer": "转座子标签法(Transposon Tagging)是一种分子生物学技术,它利用转座子(transposons)在基因组中随机插入的特性来标记和识别基因。这种方法可以帮助研究者确定基因的功能和调控机制。", "images": [], "results": [ { "title": "转座子标签法原理 - 生物通", "url": "http://www.bioon.com/article/1320/2013/09/132020130923.htm", "content": "转座子标签法是一种分子生物学技术,它利用转座子在基因组中随机插入的特性来标记和识别基因。转座子是一类可以在基因组中自主复制和移动的DNA序列。通过转座子的插入,可以导致基因的突变,从而研究基因的功能。", "score": 0.95 }, { "title": "转座子标签法在植物基因功能研究中的应用 - 植物学报", "url": "https://kxb.cas.cn/CN/abstract/abstract37889.shtml", "content": "转座子标签法在植物基因功能研究中具有重要应用。通过转座子的随机插入,可以标记到控制特定性状的基因,进而通过遗传连锁分析确定基因的位置。", "score": 0.9 }, { "title": "转座子标签法的原理和应用 - 生物谷", "url": "https://www.bioon.com/article/1320/2013/09/132020130923.htm", "content": "转座子标签法的原理基于转座子的随机插入,这种插入可以导致基因的突变,从而为研究基因功能提供了一种工具。", "score": 0.85 } ], "response_time": 1.54}
继续提问
Qianwen回答
转座子标签法(Transposon Tagging)是一种用于基因功能研究的技术,主要利用转座子(Transposons)的特性来插入目标基因组中,从而实现对基因的功能分析。以下是转座子标签法的基本原理及其应用步骤:
转座子标签法的基本原理
-
转座子的定义:
- 转座子是一段能够从一个位置移动到另一个位置的DNA序列,这种移动过程称为转座。
- 转座子可以分为两类:一类是自主转座子,自身携带转座酶基因;另一类是非自主转座子,依赖其他转座子提供的转座酶进行转座。
-
转座子的插入机制:
- 转座子通过转座酶的作用,可以从一个DNA位置跳到另一个位置。
- 插入过程中,转座子通常会在目标位点造成小片段的重复序列(称为靶标位点重复,TSD)。
-
标签的使用:
- 在转座子中插入一段已知的标记序列(标签),如抗性基因或报告基因。
- 这个标签可以帮助研究人员追踪转座子的插入位置和表达情况。
应用步骤
-
构建转座子载体:
- 设计并构建包含标签的转座子载体。
- 常见的标签包括抗生素抗性基因(如卡那霉素抗性基因)、荧光蛋白基因(如GFP)等。
-
引入转座子:
- 将转座子载体通过转化、转导或转染等方法引入目标生物细胞中。
- 转座子在转座酶的作用下随机插入基因组中的不同位置。
-
筛选插入事件:
- 利用标签基因进行筛选,选择含有转座子插入的细胞。
- 例如,使用抗生素抗性基因筛选出抗性的菌落,或使用荧光蛋白基因筛选出荧光细胞。
-
鉴定插入位点:
- 通过PCR、测序等方法确定转座子插入的具体位置。
- 分析插入位点附近的基因,确定被插入的基因及其功能。
-
功能分析:
- 研究插入位点附近基因的功能,如基因敲除、过表达等。
- 观察插入事件对细胞表型的影响,验证基因的功能。
优势和应用
- 高通量筛选:转座子标签法可以实现大规模的基因功能筛选,适用于高通量研究。
- 功能验证:通过插入位点的鉴定,可以直接验证基因的功能。
- 遗传操作:可以在多种生物中应用,包括细菌、酵母、植物和动物细胞。
参考资料
希望这些信息能帮助你更好地理解转座子标签法的原理和应用。如果你有更多具体的问题,欢迎继续提问!
继续提问
Doubao回答
转座子标签法分离克隆基因的原理主要基于转座子随机插入基因组的特性。
转座子能够随机插入到基因组的不同位置。当转座子插入到一个功能基因内部或其附近时,可能会导致该基因的功能丧失或改变,从而产生相应的突变表型。
通过观察突变表型,可以初步确定与该表型相关的基因可能被转座子插入。然后,利用转座子上携带的已知标签序列(如抗性基因、报告基因等)设计引物进行 PCR 扩增,或者通过杂交等方法来追踪转座子在基因组中的插入位置。
确定插入位置后,就可以对该区域的基因进行克隆和进一步的研究。这种方法能够有效地从庞大的基因组中定位和分离出与特定表型相关的基因。
如果您想了解更多关于基因克隆或转座子的相关知识,请随时提问。
继续提问
Baichuan回答
转座子标签法分离克隆基因是一种分子生物学技术,它利用转座子(一类能够移动的DNA片段)作为基因标记来克隆和分离特定基因。以下是该方法的原理简述:
-
转座子的特性:转座子是一种可以在DNA上“跳跃”的遗传元素,它可以将自己插入到基因组的不同位置。转座子插入时,有时会破坏或改变宿主基因的功能,这可以用来筛选特定的基因。
-
转座子库的构建:首先,科学家会将一种特殊的转座子(含有抗药性标记或其他筛选标记)随机插入到宿主细胞的基因组中,构建一个转座子库。这个库包含了许多细胞,每个细胞中的转座子都可能位于不同的基因位点。
-
筛选阳性克隆:随后,通过对这些细胞进行特定的筛选压力(如使用抗生素),选择出那些转座子插入了目标基因的细胞克隆。因为转座子带有筛选标记,只有那些转座子插入到目标基因附近的细胞才能存活或表现出特定的表型。
-
基因定位和克隆:一旦筛选到阳性克隆,就可以通过PCR(聚合酶链式反应)、测序或其他分子生物学方法来确定转座子插入的位置,从而定位目标基因。接着,可以通过进一步的实验操作(如亚克隆等)将目标基因从基因组中克隆出来,用于后续的功能分析、表达研究等。
这种技术的优点在于它能够高效地从庞大的基因库中筛选和克隆特定的基因,同时也能提供有关基因功能和位置的重要信息。转座子标签法在模式生物的遗传研究、人类疾病的基因发现以及药物开发等领域都有广泛的应用。
继续提问
参考资料



Moonshot回答
转座子标签法分离克隆基因的原理涉及以下几个关键步骤:
-
转座子插入引起的突变:转座子随机插入基因组中,可能导致基因失活或产生突变表型。这种插入是可遗传的,并且可以在后代中观察到。
-
筛选突变体:通过观察表型变化筛选出含有转座子插入的突变体。
-
转座子作为标签:转座子携带已知的标记基因(如抗性基因或报告基因),使得插入事件可以被追踪和选择。
-
基因文库构建和筛选:构建包含转座子的基因文库,并筛选出包含转座子的克隆。
-
确定插入位点:利用转座子序列作为探针,通过分子生物学技术(如PCR、Southern blot等)确定转座子在基因组中的确切插入位置。
-
克隆相邻基因:一旦确定了转座子的插入位点,就可以克隆并研究相邻的基因。
-
功能研究:对克隆的基因进行进一步的功能研究,如基因表达分析、蛋白质功能研究等。
转座子标签法的优势在于能够直接将表型变化与基因组中的特定区域联系起来,从而加速基因的克隆和功能研究。这种方法在植物基因功能研究中尤为重要,因为它允许研究者在没有预先知道基因序列的情况下克隆基因。通过转座子标签法,可以有效地分离和克隆控制特定生物学过程的基因。
继续提问
Qianwen回答
转座子标签法(Transposon Tagging)是一种有效的基因克隆和功能研究方法,通过利用转座子的插入特性来分离和克隆特定基因。以下是详细的原理和步骤:
原理概述
-
转座子的特性:
- 转座子是一段能够从一个DNA位置移动到另一个位置的DNA序列。
- 转座子的移动(转座)由转座酶催化,可以在基因组中随机插入。
- 转座子插入时,通常会在插入点产生小片段的重复序列(靶标位点重复,TSD)。
-
标签的使用:
- 转座子中包含一个已知的标记序列(标签),如抗生素抗性基因、荧光蛋白基因等。
- 这个标签可以帮助研究人员追踪转座子的插入位置和表达情况。
应用步骤
-
构建转座子载体:
- 设计并构建包含标签的转座子载体。
- 常见的标签包括抗生素抗性基因(如卡那霉素抗性基因)、荧光蛋白基因(如GFP)等。
-
引入转座子:
- 将转座子载体通过转化、转导或转染等方法引入目标生物细胞中。
- 转座子在转座酶的作用下随机插入基因组中的不同位置。
-
筛选插入事件:
- 利用标签基因进行筛选,选择含有转座子插入的细胞。
- 例如,使用抗生素抗性基因筛选出抗性的菌落,或使用荧光蛋白基因筛选出荧光细胞。
-
鉴定插入位点:
- 通过PCR、测序等方法确定转座子插入的具体位置。
- 分析插入位点附近的基因,确定被插入的基因及其功能。
-
分离克隆目标基因:
- 一旦确定了转座子插入的目标基因位置,可以通过基因克隆技术将目标基因从基因组中分离出来。
- 使用限制性内切酶切割基因组DNA,通过凝胶电泳分离目标片段。
- 将目标片段连接到合适的载体中,进行克隆和扩增。
详细步骤
-
构建转座子载体:
- 选择合适的转座子系统,如Tn5、Ac/Ds、P-element等。
- 在转座子中插入标记基因,如抗生素抗性基因(如kanR)或荧光蛋白基因(如GFP)。
-
引入转座子:
- 将构建好的转座子载体通过转化、转导或转染等方法引入目标生物细胞中。
- 例如,在细菌中使用电穿孔法或化学转化法,在植物中使用农杆菌介导的转化法。
-
筛选插入事件:
- 将转化后的细胞接种到含有相应抗生素的选择培养基上,筛选出抗性的菌落。
- 或者使用荧光显微镜筛选出表达荧光蛋白的细胞。
-
鉴定插入位点:
- 从筛选出的阳性克隆中提取基因组DNA。
- 使用特异性引物进行PCR扩增,扩增转座子两侧的基因组序列。
- 对PCR产物进行测序,确定转座子插入的具体位置。
-
分离克隆目标基因:
- 根据测序结果设计特异性引物,扩增目标基因的完整序列。
- 使用限制性内切酶切割PCR产物,将目标基因片段插入到合适的载体中。
- 转化大肠杆菌,筛选阳性克隆,进行序列验证。
优势和应用
- 高通量筛选:转座子标签法可以实现大规模的基因功能筛选,适用于高通量研究。
- 功能验证:通过插入位点的鉴定,可以直接验证基因的功能。
- 遗传操作:可以在多种生物中应用,包括细菌、酵母、植物和动物细胞。
参考资料
希望这些信息能帮助你更好地理解转座子标签法分离克隆基因的原理和应用。如果你有更多具体的问题,欢迎继续提问!
继续提问
Doubao回答
要确保 ISSR(Inter Simple Sequence Repeat,简单序列重复区间扩增多态性)PCR 过程中扩增范围不会过大,可以考虑以下几个方面:
-
引物设计:选择合适的 ISSR 引物非常关键。引物的长度、序列和退火温度等特性会影响扩增的特异性和范围。通常,精心设计的引物能够与特定的基因组区域结合,从而限制扩增范围。
-
退火温度优化:通过实验优化退火温度。较高的退火温度可以增加引物与目标序列结合的特异性,减少非特异性扩增,从而控制扩增范围。
-
镁离子浓度:调整镁离子的浓度。适当的镁离子浓度有助于提高 PCR 反应的特异性和准确性,防止过度扩增。
-
PCR 循环数:控制 PCR 循环数。过多的循环数可能导致过度扩增,应根据实验需求和模板量选择合适的循环数。
-
模板质量和浓度:使用高质量、高纯度的 DNA 模板,并控制模板的浓度。过高的模板浓度可能导致非特异性扩增和扩增范围过大。
-
反应条件的严格性:保持反应条件的严格性,如使用高质量的 PCR 试剂、精确控制反应温度和时间等。
-
预实验和梯度测试:在正式实验前进行预实验和梯度测试,以确定最佳的反应条件,包括引物浓度、退火温度、镁离子浓度等,从而确保扩增范围在预期之内。
-
监控 PCR 产物:在 PCR 过程中,可以通过琼脂糖凝胶电泳等方法定期监测 PCR 产物的大小和量,及时发现并调整可能导致扩增范围过大的因素。
通过综合考虑和优化以上因素,可以有效地确保 ISSR PCR 过程中扩增范围在可控范围内,获得准确和可靠的实验结果。
继续提问
Baichuan回答
ISSR(Inter Simple Sequence Repeat,即简单序列间重复)是一种分子标记技术,它利用简单重复序列(如CA、AG等)之间的区域作为PCR(聚合酶链式反应)扩增的靶标。为了确保PCR过程中扩增范围不会过大,ISSR技术采取以下措施:
-
引物设计:ISSR技术使用的引物是根据已知的简单重复序列设计的,这些引物与基因组DNA中的简单重复序列互补。通过调整引物的长度和碱基序列,可以控制PCR扩增的特异性和效率,从而避免扩增范围过大。
-
优化反应体系:通过优化PCR反应体系中的各种成分(如DNA聚合酶、Mg²⁺浓度、dNTPs浓度等),可以提高PCR扩增的特异性和效率,减少非特异性扩增,从而避免扩增范围过大。
-
选择合适的退火温度:通过选择合适的退火温度,可以提高引物与模板DNA的特异性结合,减少非特异性扩增,从而避免扩增范围过大。
-
控制循环次数:通过控制PCR循环次数,可以限制扩增产物的数量,从而避免扩增范围过大。一般来说,循环次数越多,扩增范围越广;循环次数越少,扩增范围越小。
-
选择适当的模板DNA:选择高质量、高纯度的模板DNA,可以提高PCR扩增的特异性和效率,减少非特异性扩增,从而避免扩增范围过大。
通过以上措施,ISSR技术可以在保证扩增效率和特异性的前提下,有效地避免扩增范围过大。
继续提问
Moonshot回答
functions.search:1$ { "max_results": 3, "query": "ISSR PCR扩增范围控制", "search_depth": "basic" } ['$']:1 { "query": "ISSR PCR扩增范围控制", "follow_up_questions": [], "answer": "在进行ISSR(Inter-Simple Sequence Repeat)PCR时,确保扩增范围不会过大通常涉及以下几个方面:\n1. 引物设计:选择合适的引物,避免过长或复杂的引物序列,以减少非特异性扩增。\n2. 退火温度:优化退火温度,确保引物与模板DNA的特异性结合。\n3. 循环次数:合理设置循环次数,避免过度循环导致非特异性扩增。\n4. PCR产物分析:通过凝胶电泳分析PCR产物,筛选出目标片段。\n以上方法可以帮助控制ISSR PCR过程中的扩增范围,提高实验的准确性和可重复性。", "images": [], "results": [ { "title": "ISSR-PCR技术原理及其在遗传多样性研究中的应用", "url": "http://www.ckhk.net/Article/43539", "content": "ISSR-PCR技术是一种基于微卫星的分子标记技术,通过非特异性引物与微卫星序列互补结合,扩增微卫星两侧的DNA片段。在实验中,需要严格控制反应条件,以确保扩增范围不会过大。" }, { "title": "PCR扩增范围控制方法", "url": "https://www.bio-tech.com/Article/2019/03/04/45663.htm", "content": "在PCR扩增过程中,可以通过优化引物设计、调整退火温度和循环次数等方法来控制扩增范围。" }, { "title": "ISSR-PCR实验操作注意事项", "url": "https://www.bio-online.com/con_info_detail/40134", "content": "在进行ISSR-PCR实验时,需要注意引物的浓度、Mg2+的浓度、dNTPs的浓度等因素,以确保实验结果的稳定性和可靠性。" } ], "response_time": 1.21}
继续提问
Qianwen回答
ISSR (Inter-Simple Sequence Repeat) 是一种基于PCR的分子标记技术,用于检测基因组中简单重复序列之间的多态性。为了确保PCR过程中扩增范围不会过大,通常采取以下几种措施:
1. 选择合适的引物
- 引物设计:选择长度适中、GC含量合理的引物。通常,ISSR引物长度在15-20个碱基之间,GC含量在40%-60%之间。
- 引物特异性:确保引物能够特异性地结合到目标区域,避免非特异性扩增。可以通过BLAST等工具检查引物的特异性。
2. 优化PCR反应条件
- 退火温度:选择合适的退火温度,通常在50-60°C之间。较高的退火温度可以减少非特异性扩增。
- 循环次数:控制PCR循环次数,通常在25-35个循环之间。过多的循环次数会导致非特异性扩增。
- 延伸时间:调整延伸时间,通常在1-2分钟之间。过长的延伸时间可能导致扩增产物过大。
3. 控制模板DNA的浓度
- 模板浓度:确保模板DNA的浓度适中,过高或过低的模板浓度都可能导致非特异性扩增。通常,模板DNA的浓度在10-50 ng/μL之间。
4. 使用高保真DNA聚合酶
- 聚合酶选择:使用高保真DNA聚合酶,如Pfu DNA聚合酶,可以提高扩增的特异性和准确性,减少非特异性扩增。
5. 添加PCR添加剂
- 添加剂:添加PCR添加剂,如DMSO、BSA等,可以改善PCR反应的特异性。DMSO可以降低DNA的二级结构,BSA可以保护酶的活性。
6. 优化反应缓冲液
- 缓冲液:使用优化的PCR缓冲液,可以提高PCR反应的效率和特异性。不同的聚合酶可能需要不同的缓冲液条件。
7. 严格控制实验条件
- 实验条件:保持实验条件的一致性,如温度、时间和试剂批次,可以减少实验误差。
实际操作步骤
-
引物设计:
- 使用在线工具(如Primer3)设计ISSR引物。
- 检查引物的特异性(如使用BLAST)。
-
PCR反应体系:
- 模板DNA:10-50 ng/μL
- 引物:0.2-0.5 μM
- dNTPs:0.2 mM
- MgCl2:1.5-2.5 mM
- 高保真DNA聚合酶:1-2 U
- PCR缓冲液:1X
- DMSO(可选):5-10%
- BSA(可选):0.1 mg/mL
- 总体积:25 μL
-
PCR反应程序:
- 初始变性:94°C,3分钟
- 循环变性:94°C,30秒
- 退火:50-60°C,30秒
- 延伸:72°C,1-2分钟
- 最终延伸:72°C,10分钟
- 4°C保存
通过以上措施,可以有效控制PCR过程中扩增范围,确保ISSR技术的准确性和可靠性。希望这些信息对你有所帮助!如果有更多具体问题,欢迎继续提问。
继续提问
Baichuan回答
ISSR(Inter Simple Sequence Repeat)是一种分子标记技术,通过特异性的引物结合在简单序列重复区域间的非重复区,实现对特定DNA区段的扩增。在PCR(聚合酶链式反应)过程中,ISSR引物是如何实现特异性结合的呢?
-
设计引物:ISSR引物基于简单重复序列(如微卫星)之间的非重复区设计而成。这意味着引物与DNA上的非重复区具有很高的互补性。
-
退火阶段:在PCR反应的退火阶段,引物会与模板DNA上的互补序列特异性结合。由于引物是基于非重复区设计的,因此它们只会与模板DNA上的特定区域结合。
-
延伸阶段:在PCR反应的延伸阶段,DNA聚合酶沿着引物启动的部位合成新的DNA链。因为引物特异性地结合在特定的非重复区域,所以新合成的DNA链也是特定于这一区域的。
-
循环重复:随着PCR循环的重复,特异性扩增的DNA区段数量呈指数级增长。这样,即使原始模板DNA中的非重复区域只有一小段,也能通过ISSR-PCR技术被大量扩增出来。
因此,ISSR引物通过特异性的设计以及PCR过程中的退火和延伸步骤,能够实现在PCR过程中对特定DNA区段的高度特异性结合和扩增。这种特异性结合使得ISSR技术成为研究基因多样性、种群遗传结构和亲缘关系分析的重要工具之一。
继续提问
Claude回答
ISSR在PCR过程中实现特异性结合主要通过以下几个方面:
1. 引物设计
- 引物序列:
- 包含重复序列(如(AG)n, (CT)n等)
- 在3'端添加1-3个选择性碱基(锚定核苷酸)
- 这些锚定核苷酸能确保引物只与特定的微卫星序列结合
2. 优化PCR条件
-
退火温度:
- 使用较高的退火温度(通常45-60℃)
- 可以采用梯度PCR找到最佳退火温度
- 高退火温度能减少非特异性结合
-
Mg2+浓度:
- 控制Mg2+浓度在1.5-2.5 mM
- Mg2+影响引物与模板的结合特异性
- 过高浓度会导致非特异性扩增
3. 反应体系优化
-
引物浓度:
- 控制在0.2-0.5 μM
- 避免过高浓度导致引物自身配对
-
模板DNA质量:
- 使用高质量的模板DNA
- DNA浓度保持在20-50 ng/μL
- 确保DNA纯度(A260/A280比值在1.8-2.0)
4. 添加优化剂
- DMSO:降低DNA二级结构
- 甜菜碱:提高PCR特异性
- BSA:稳定酶活性
通过以上措施的综合运用,可以显著提高ISSR-PCR的特异性。
followup
end
继续提问
Baichuan回答
ISSR(Inter-Simple Sequence Repeat)是一种分子标记技术,它利用微卫星序列(简单序列重复,如CA重复)之间的DNA区域作为标记。ISSR技术通过PCR(聚合酶链式反应)扩增这些区域来进行基因组分析。
在PCR过程中,ISSR的特异性结合主要通过以下方式实现:
-
引物设计:ISSR引物是根据微卫星序列的保守区设计的。引物通常设计在微卫星序列的两侧,使得PCR能够扩增包含微卫星序列的DNA片段。
-
引物退火:在PCR的退火步骤中,引物与模板DNA上的互补序列结合。由于引物是根据微卫星序列的保守区设计的,因此引物只能与包含该微卫星序列的DNA片段结合,从而实现特异性结合。
-
扩增特异性片段:通过PCR的多个循环,引物引导的DNA合成只会在包含微卫星序列的DNA片段上进行,从而扩增这些特异性片段。
通过以上步骤,ISSR技术能够在PCR过程中实现特异性结合,从而用于基因组分析、遗传多样性分析、基因定位等方面。
继续提问
Doubao回答
ISSR(Inter Simple Sequence Repeat)在 PCR 过程中实现特异性结合主要通过以下几个方面:
-
引物设计:ISSR 引物是根据基因组中简单序列重复(SSR)两侧的保守区域设计的。这些引物具有特定的碱基序列,能够与目标区域的 DNA 模板互补配对。
-
退火温度:在 PCR 反应中,设置合适的退火温度至关重要。退火温度足够高时,只有与引物完全互补的模板 DNA 区域才能稳定结合,非特异性结合会因不稳定而解离,从而保证引物的特异性结合。
-
碱基互补配对:引物与模板 DNA 之间严格的碱基互补配对是特异性结合的基础。只有当引物的碱基序列与模板的相应区域完全互补时,才能形成稳定的双链结构。
-
反应条件优化:包括 PCR 缓冲液的成分、Mg2+浓度等,合适的反应条件有助于提高引物结合的特异性。
-
模板纯度:高质量、高纯度的模板 DNA 可以减少杂质对引物结合的干扰,增强特异性结合。
综上所述,通过精心设计引物、优化反应条件和保证模板质量,ISSR 能够在 PCR 过程中实现特异性结合,从而准确扩增出目标 DNA 片段。
如果您想进一步了解相关内容或还有其他疑问,请继续提问。
继续提问
Claude回答
ISSR在PCR过程中实现特异性结合主要通过以下几个方面:
1. 引物设计
- 序列设计:
- 引物通常包含重复序列(如(AG)n, (CT)n等)
- 在3'端添加1-3个选择性碱基,提高特异性
- 引物长度一般为16-25个核苷酸
- 控制GC含量在40-60%之间
2. 反应条件优化
-
退火温度:
- 使用较高的退火温度(45-60℃)
- 可以进行温度梯度实验找到最佳退火温度
- 温度越高,结合特异性越强
-
Mg²⁺浓度:
- 控制在1.5-2.5 mM之间
- Mg²⁺浓度影响引物与模板的结合稳定性
3. PCR反应体系
-
模板DNA质量:
- 使用高质量、纯度好的DNA模板
- 控制模板浓度在20-50ng/μL
-
引物浓度:
- 通常控制在0.2-0.4μM
- 避免过高浓度导致非特异性结合
4. 反应程序优化
-
预变性:
- 94-95℃,3-5分钟
- 充分解开DNA双链
-
循环条件:
- 变性:94℃,30-45秒
- 退火:根据引物设计温度,30-45秒
- 延伸:72℃,1-2分钟
- 循环数:30-35次
5. 质量控制
- 使用阴性对照确认无污染
- 通过琼脂糖凝胶电泳检测扩增产物
- 必要时进行测序验证
通过以上措施的综合运用,可以确保ISSR-PCR的特异性结合,获得可靠的实验结果。
followup
end
继续提问
Baichuan回答
functions.search:2$ { "max_results": 3, "query": "ISSR PCR特异性结合", "search_depth": "basic" } ['$']:2 { "query": "ISSR PCR特异性结合", "follow_up_questions": [], "answer": "在ISSR(Inter-Simple Sequence Repeat)PCR中,特异性结合主要通过以下方式实现:\n1. 引物设计:ISSR引物是根据微卫星序列设计的,与微卫星两侧的非重复序列互补。这种设计使得引物只能与特定的DNA序列结合,从而实现特异性扩增。\n2. 退火温度:通过优化退火温度,可以提高引物与模板DNA的特异性结合,避免非特异性扩增。\n3. 循环次数:适当控制循环次数,可以减少非特异性扩增,提高PCR产物的特异性。\n4. 凝胶电泳分析:通过凝胶电泳分析PCR产物,可以筛选出目标片段,进一步提高特异性。\n综上所述,通过引物设计、退火温度优化、循环次数控制和凝胶电泳分析等方法,ISSR PCR可以实现特异性结合和扩增。", "images": [], "results": [ { "title": "ISSR-PCR技术原理及其在遗传多样性研究中的应用", "url": "http://www.ckhk.net/Article/43539", "content": "ISSR-PCR技术是一种基于微卫星的分子标记技术,通过非特异性引物与微卫星序列互补结合,扩增微卫星两侧的DNA片段。在实验中,需要严格控制反应条件,以确保扩增范围不会过大。" }, { "title": "PCR扩增范围控制方法", "url": "https://www.bio-tech.com/Article/2019/03/04/45663.htm", "content": "在PCR扩增过程中,可以通过优化引物设计、调整退火温度和循环次数等方法来控制扩增范围。" }, { "title": "ISSR-PCR实验操作注意事项", "url": "https://www.bio-online.com/con_info_detail/40134", "content": "在进行ISSR-PCR实验时,需要注意引物的浓度、Mg2+的浓度、dNTPs的浓度等因素,以确保实验结果的稳定性和可靠性。" } ], "response_time": 1.21}
继续提问
Moonshot回答
functions.search:2$ { "max_results": 5, "query": "ISSR PCR 特异性结合", "search_depth": "basic" } ['$']:2 { "query": "ISSR PCR 特异性结合", "follow_up_questions": [], "answer": "ISSR(Inter-Simple Sequence Repeat)技术在PCR过程中实现特异性结合主要依赖于以下几点:\n1. 引物设计:ISSR引物通常设计为与简单序列重复(SSR)两侧的保守区域互补,以确保引物与目标DNA区域特异性结合。\n2. 退火温度:通过优化退火温度,可以提高引物与模板DNA的特异性结合,减少非特异性扩增。\n3. 循环次数:合理设置循环次数,避免过度循环导致非特异性扩增。\n4. PCR产物分析:通过凝胶电泳分析PCR产物,筛选出目标片段。\n以上方法可以帮助控制ISSR PCR过程中的扩增范围,提高实验的准确性和可重复性。", "images": [], "results": [ { "title": "ISSR-PCR技术原理及其在遗传多样性研究中的应用", "url": "http://www.ckhk.net/Article/43539", "content": "ISSR-PCR技术是一种基于微卫星的分子标记技术,通过非特异性引物与微卫星序列互补结合,扩增微卫星两侧的DNA片段。在实验中,需要严格控制反应条件,以确保扩增范围不会过大。" }, { "title": "PCR扩增范围控制方法", "url": "https://www.bio-tech.com/Article/2019/03/04/45663.htm", "content": "在PCR扩增过程中,可以通过优化引物设计、调整退火温度和循环次数等方法来控制扩增范围。" }, { "title": "ISSR-PCR实验操作注意事项", "url": "https://www.bio-online.com/con_info_detail/40134", "content": "在进行ISSR-PCR实验时,需要注意引物的浓度、Mg2+的浓度、dNTPs的浓度等因素,以确保实验结果的稳定性和可靠性。" }, { "title": "ISSR引物设计原则", "url": "https://www.researchgate.net/publication/329696381_Inter-Simple_Sequence_Repeat_Marker_Development_and_Application", "content": "ISSR引物设计原则包括:引物与微卫星序列两侧的保守区域互补;引物长度适中;GC含量平衡;避免引物二聚体和发夹结构。" }, { "title": "PCR反应条件优化", "url": "https://www.sciencedirect.com/science/article/pii/S2452199420300248", "content": "PCR反应条件优化包括:引物浓度、Mg2+浓度、dNTPs浓度、退火温度、循环次数等。" } ], "response_time": 1.05}
继续提问
Qianwen回答
ISSR(Inter-Simple Sequence Repeat)PCR技术通过一系列精心设计的步骤来实现特异性结合,从而确保扩增的DNA片段是特定的。以下是具体的实现方法:
1. 引物设计
- 引物选择:ISSR引物通常基于简单重复序列(如CA、GT等)设计。这些引物在基因组中具有多个潜在的结合位点,但通过选择特定的简单重复序列和适当的引物长度,可以提高特异性。
- 引物长度:引物长度通常在15-20个碱基之间。较长的引物可以增加特异性,减少非特异性结合。
- GC含量:引物的GC含量通常在40%-60%之间,以确保引物在退火过程中与模板DNA的结合稳定性。
2. 退火温度优化
- 退火温度:选择合适的退火温度是确保特异性结合的关键。较高的退火温度可以减少非特异性结合,提高引物与模板DNA的特异性结合。通常,退火温度在50-60°C之间。
- 梯度PCR:可以通过梯度PCR来确定最佳的退火温度。梯度PCR可以在同一个反应中测试多个退火温度,从而找到最优的退火条件。
3. 控制PCR反应条件
- Mg²⁺浓度:Mg²⁺是DNA聚合酶的辅助因子,适当的Mg²⁺浓度可以提高PCR的特异性。通常,Mg²⁺浓度在1.5-2.5 mM之间。
- dNTPs浓度:适当的dNTPs浓度可以确保PCR反应的顺利进行,过高或过低的dNTPs浓度都可能导致非特异性扩增。通常,dNTPs浓度在0.2 mM左右。
- 模板DNA浓度:使用高质量、高纯度的模板DNA,并控制模板DNA的浓度。过高的模板浓度可能导致非特异性扩增。通常,模板DNA的浓度在10-50 ng/μL之间。
4. 使用高保真DNA聚合酶
- 聚合酶选择:使用高保真DNA聚合酶,如Pfu DNA聚合酶,可以提高扩增的特异性和准确性,减少非特异性扩增。
5. 添加PCR添加剂
- DMSO:DMSO可以降低DNA的二级结构,提高引物与模板DNA的结合效率。通常,DMSO的浓度在5-10%之间。
- BSA:BSA可以保护酶的活性,提高PCR反应的特异性。通常,BSA的浓度在0.1 mg/mL左右。
6. 优化PCR反应程序
- 初始变性:94°C,3分钟,以确保模板DNA完全变性。
- 循环变性:94°C,30秒,使双链DNA完全分离。
- 退火:50-60°C,30秒,使引物与模板DNA特异性结合。
- 延伸:72°C,1-2分钟,使DNA聚合酶合成新的DNA链。
- 最终延伸:72°C,10分钟,确保所有DNA链完全合成。
- 保存:4°C,保存扩增产物。
7. 通过凝胶电泳验证
- 凝胶电泳:通过凝胶电泳分析PCR产物,可以直观地看到扩增产物的大小和特异性。如果出现非特异性条带,可以通过调整上述条件来优化反应。
通过以上措施,ISSR PCR技术可以实现高度特异性的结合,从而确保扩增的DNA片段是特定的。希望这些信息能帮助你更好地理解和应用ISSR技术。
followup
end
继续提问
Claude回答
ISSR (Inter-Simple Sequence Repeat) PCR扩增过程中,为了确保扩增范围适中,可以采取以下措施:
- 引物设计优化:
- 选择合适长度的引物(通常16-25个碱基)
- 引物中包含2-4个锚定核苷酸
- 确保引物GC含量适中(40-60%)
- PCR反应条件控制:
- 优化退火温度:通常设置在45-65℃之间
- 使用梯度PCR找到最佳退火温度
- 控制延伸时间:通常1-2分钟即可
- 反应体系优化:
- 调整模板DNA浓度(20-50ng/μL)
- 控制Mg2+浓度(通常1.5-2.5mM)
- 适当的dNTPs浓度(每种0.2mM左右)
- 循环参数调整:
- 控制循环数(通常30-35个循环)
- 适当的变性时间(94℃,30-60秒)
- 合适的延伸温度(72℃)
- 质量控制:
- 使用高质量的模板DNA
- 选择合适的DNA聚合酶
- 设置阴性对照确保结果可靠
通过以上措施的综合运用,可以有效控制ISSR-PCR的扩增范围,获得清晰的条带图谱。
followup
end