如何利用热力学第二定律解释物质的自发变化趋势?
参考资料


Moonshot回答
热力学第二定律是热力学的四条基本定律之一,它描述了热力学过程的不可逆性。根据这一定律,孤立系统自发地朝着热力学平衡方向——最大熵状态——演化。这意味着在一个孤立系统中,物质的自发变化趋势总是向着熵增的方向进行。
熵是一个物理量,用来衡量系统的无序程度。熵增原理表明,在一个孤立系统中,熵不会自发减少,系统总是自发地向更无序的状态发展。例如,在等温、等压或等温、等容条件下进行的化学反应,总是倾向于向生成更多产物的方向进行,因为这样系统的总熵会增加。
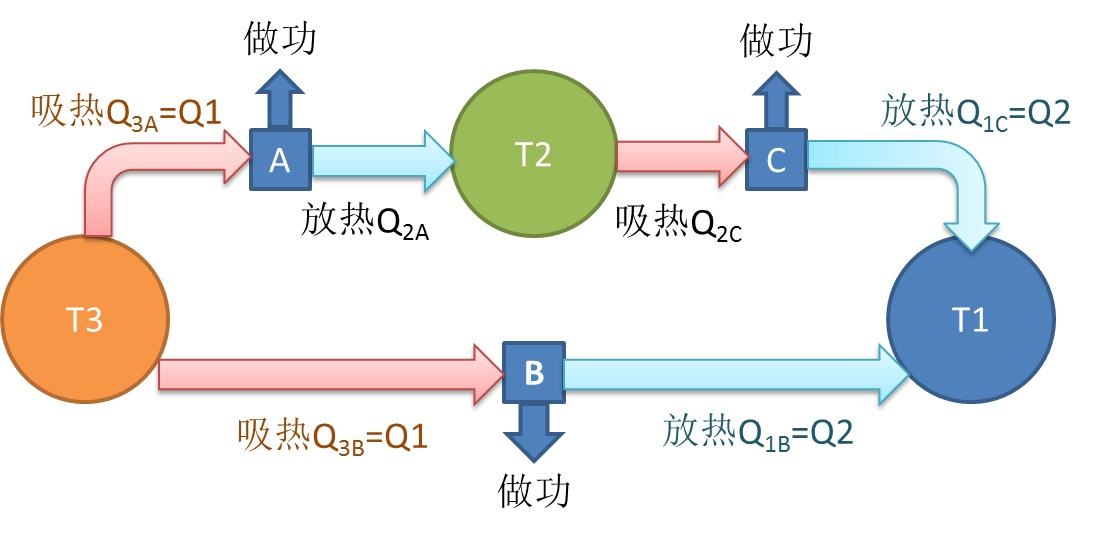
热力学第二定律还揭示了热量与功的转化以及热量传递的不可逆性。例如,热量自然地从高温物体传递到低温物体,而不会自发地反向传递。这也意味着第二类永动机(从单一热源吸热完全转化为功而不产生其他效果的机器)是不可能实现的。
通过引用的搜索结果,我们可以看到热力学第二定律的表述和解释,以及它如何应用于判断物质的自发变化趋势。例如,维基百科上的解释说明了自发过程总是从热力学概率小的状态向热力学概率大的状态转变,这与熵增原理是一致的。此外,还有图像资料展示了与热力学第二定律相关的物理过程和概念,如热量传递和熵变。
总结来说,热力学第二定律通过熵的概念,解释了物质的自发变化趋势总是向着熵增的方向进行,即系统自发地向更无序的状态发展。这一原理适用于各种物理和化学过程,是理解和预测物质行为的重要工具。